順天堂大学(東京都文京区)の研究グループは2026年5月5日、p62が作る凝集体の性質がリン酸化で変わり、ユビキチン化タンパク質をオートファジー(細胞の分解・再利用機構)で分解する効率が決まる仕組みを示しました。成果はEMBO Journalオンライン版(同日付)に掲載され、DOIは10.1038/s44318-026-00785-1です。
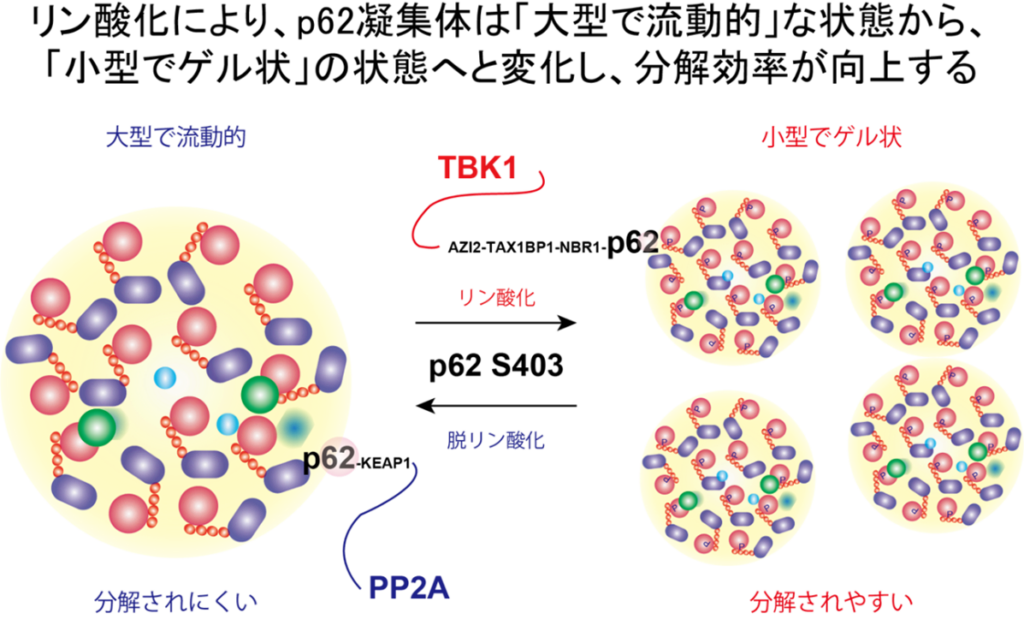
p62は不要になったタンパク質に付く「ユビキチン」を目印に集め、凝集体(p62ボディ)としてまとめて分解へ導く因子ですが、どの状態の凝集体が分解されやすいかは不明でした。研究では、リン酸化部位Ser403が鍵になると位置付けました。
順天堂大学大学院医学研究科(器官・細胞生理学)の小松雅明主任教授らは、培養細胞解析、in vitro再構成実験、顕微鏡観察、遺伝子改変マウス解析を組み合わせ、TBK1とPP2AによるSer403のリン酸化制御を検証しました。その結果、p62凝集体が流動的状態からコンパクトで安定な状態へ移行し、膜構造との相互作用が促進されることで分解効率が高まることを示しました。
同成果は、分解対象側の「物性制御」という視点からタンパク質品質管理機構の理解を進め、神経変性疾患やがんなど異常タンパク質蓄積を特徴とする病態での役割解明を経て、新たな治療戦略の検討につながる可能性があります。
【関連リンク】
公式HP: http://www.juntendo.ac.jp
DOI: 10.1038/s44318-026-00785-1
AI生成記事のため誤りを含む場合があります
PRTIMES

PRTIMES
リン酸化がタンパク質分解効率を決める仕組みを解明